Inhalt
Vorbemerkung:
Offensichtlich ist es ein Menschheitstraum zu verstehen, was 'Materie' eigentlich ist:
Die griechischen Philosophen benannten Feuer, Wasser, Luft und Erde als
- das Warme und Trockene. Es steht für Energie, Geist, Umwandlung und Dynamik.
- das Kalte und Feuchte. Es steht für das Flüssige, die Fruchtbarkeit und die Formbarkeit.
- das Warme und Feuchte. Sie steht für den Atem (Pneuma), die Ausdehnung und die Verbindung zwischen Himmel und Erde.
- das Kalte und Trockene. Sie steht für das Feste, die Materie, Stabilität und die physische Basis der Welt.
- Der Begriff des Unteilbaren - atomos - wurde maßgeblich von Leukipp und seinem Schüler Demokrit im 5. Jahrhundert v. Chr. geprägt.
Jahrhunderte lang gelang der 'alten Welt' kein Fortschritt in Sachen Aufbau und Struktur der Materie. - Erst im frühen 19. Jahrhundert begründete der englische Chemiker John Dalton die moderne Atomtheorie. Er verknüpfte die philosophische Idee des Atoms mit messbaren chemischen Fakten, wie dem Gesetz der konstanten Proportionen. Er postulierte, dass jedes Element aus identischen, unteilbaren Atomen besteht, die sich bei chemischen Reaktionen neu anordnen.
- Erste konkrete Atommodelle formulierten Joseph John Thomson im Jahr 1903 und Ernest Rutherford um 1910.
- Thomson: Rosinenkuchenmodell
- Rutherford: ein sehr kleiner positiver Kern wird von noch kleineren negativ geladenen Teilchen (Elektronen) umkreist.
Beide Modelle hielten genauerer Analyse nicht stand.
Erst Niels Bohr gelang es mit seinen "Bohrschen Postulaten" ein entscheidender Fortschritt mit einer a priori-Quantelung der Elektronen-Bahnen.
Damit ließen sich etwa die Balmersche Serienformel u. a. verstehen ... noch ganz ohne Quantenphysik ... Natürlich finden auch die Fraunhoferschen Linien im Sonnenlicht Erwähnung incl. Berechnung der fehlenden Farben Platz.
zum Schluss: Bohrs Vita
 Vielleicht hatte Joseph John Thomson im Jahr 1903 (!) seine Idee vom Aufbau der Atome beim Frühstück anl. eines Besuches in München als korrespondierendes Mitglied der Bayerischen Akademie der Wissenschaften. Jedenfalls wurde seine Idee bekannt als das sogenannte Rosinenbrötchenmodell:
Vielleicht hatte Joseph John Thomson im Jahr 1903 (!) seine Idee vom Aufbau der Atome beim Frühstück anl. eines Besuches in München als korrespondierendes Mitglied der Bayerischen Akademie der Wissenschaften. Jedenfalls wurde seine Idee bekannt als das sogenannte Rosinenbrötchenmodell:
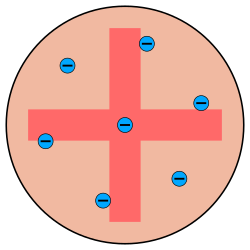 Dabei zerlegte er das elektrische neutral Atom in einen positiven Bereich, darin eingebettet die negativen Rosinen.
Dabei zerlegte er das elektrische neutral Atom in einen positiven Bereich, darin eingebettet die negativen Rosinen.
Erst John Rutherford erkannte um das Jahr 1910, dass ein Atom der Größenordnung von 10-10 m weitgehend "leer" sein musste:
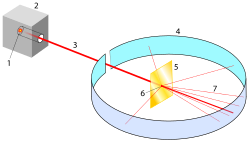 Nur etwa jedes 100.000ste Alpha-Teilchen wird um 90 Grad oder mehr abgelenkt.
Nur etwa jedes 100.000ste Alpha-Teilchen wird um 90 Grad oder mehr abgelenkt.
Also, so folgerte er, hat ein Atom einen sehr kleinen positiv geladenen Kern, welcher von sehr kleinen negativ geladenen Elektronen umkreist wird, so wie ein kleiner Satellit oder der Mond - könnten man heute sagen - die Erde umkreist, oder die Planeten die Sonne,
Nur, schon Heinrich Hertz (1857-1890) wusste seit Experimenten mit einem Dipol, dass beschleunigte Ladung Energie abstrahlt. Damit konnte das Rutherfordsche Atom nie und nimmer stabil sein, das Elektron müsste unmittelbar und sofort in den Kern stürzen. Es gäbe so überhaupt keine Materie.
Erst Niels Bohr konnte das Problem wie den berühmten gordischen Knoten mit einem Schlag, besser Postulat, lösen:
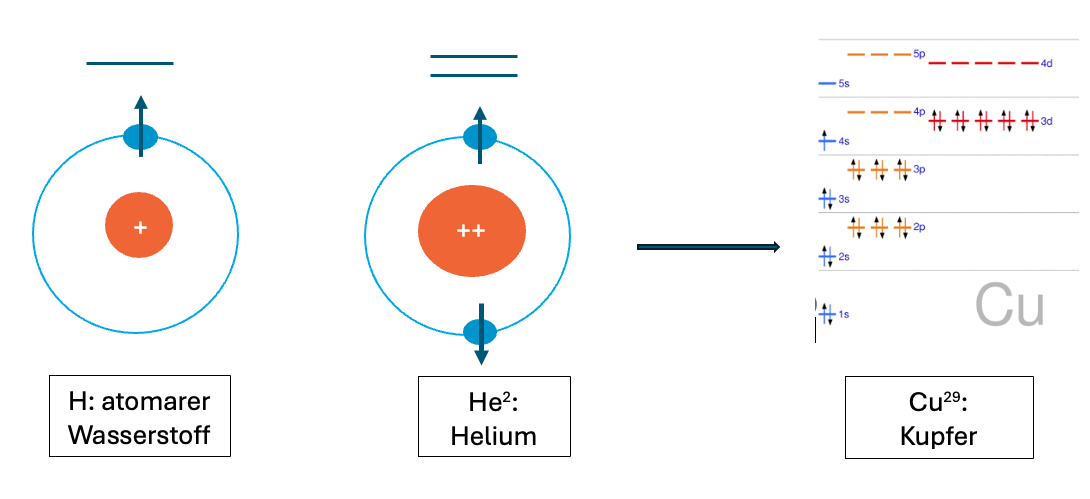
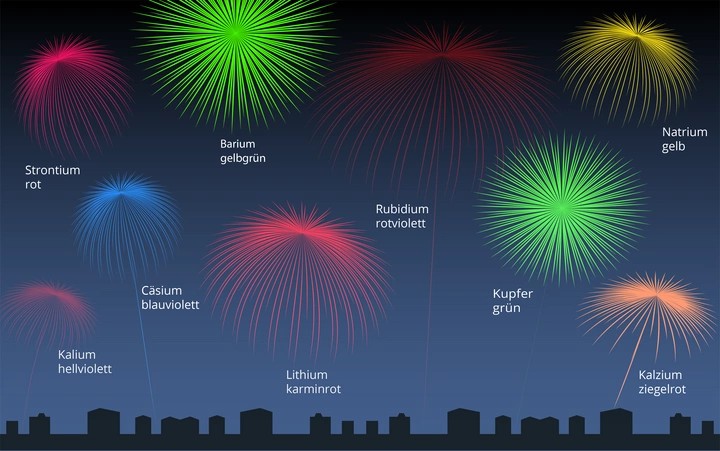
Niels Bohr: Elektronen bewegen sich auf "Schalen" strahlungsfrei, welche von "innen" nach "außen" mit 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p usw nummeriert werden. Durch Energiezufuhr könnten sie höhere Schalen erreichen strahlen diese charakteristische Energie in charakteristischen Farben ab. Zum Beispiel sorgt im Feuerwerk Kupfer für grünes Licht!
Andere 'Salze' ergeben andere Farben:
Sonnenlicht scheint weiß zu sein, weil an der Sonnenoberfläche viele Atome charakteristisches Licht abstrahlen. Manche Lichtquanten können aber die Sonne nicht verlassen. Deshalb fand Fraunhofer im Sonnenspektrum charakteristische schwarze Linien:

Die Linien entstehen überwiegend durch Resonanzabsorption der Gase in der Sonnen-Photosphäre, teilweise aber auch durch Absorption an den Gasen der Erdatmosphäre (sog. „tellurische Linien“).
Bild- und Textquelle: Wikipedia
Eine tiefere Begründung der Bohrschen Postulate lieferte die Quantenphysik mit ihren Quantenzahlen. Diese Zahlen hatte im Prinzip auch ein gewisser Johann Jakob Balmer im Jahre 1885 'erfunden'. Er fand durch Probieren eine Gesetzmäßigkeit der Spektralfarben der Wasserstoffspektrums:

Die Gesetzmäßigkeit der Wellenlängen der Balmerserie lautet:
const*(1/22 - 1/n2), n = 3, 4 ... unendlich
Die Konstante bekommt später den Namen Rydbergkonstante R, 'n' wird Hauptquantenzahl genannt werden.
Es ist doch sehr interessant, mal nachzurechnen: Übergang 2 -> n=3 mit const = 1,0973731568157 *107 m-1 ergibt mithilfe des österreichischen TermeRechners "mathespass.at/klasse3/"
und mittels ETR in nm = 10-9
656 nm , also rotes Licht!
Interessant ist sicher der Test, ob die Lösung der Gleichung 1/434 nm = R*( 1/22 - 1/x2 ) mit R=1.097083 näherungsweise eine natürlich Zahl ergibt. Aus dieser kann man dann in der Balmer-Serie den Rücksprung eines Elektron von der Schale x auf die Schale n = 2 ablesen:

Eine endgültige Begründung für das Auftreten der natürlichen Zahlen n liefert Jahrzehnte nach Bohr die Quantenphysik eines Schrödingers ...
Interessant könnte sein, wie die KI mit

umgeht? So:
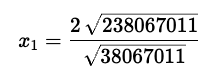
Der ETR macht daraus:
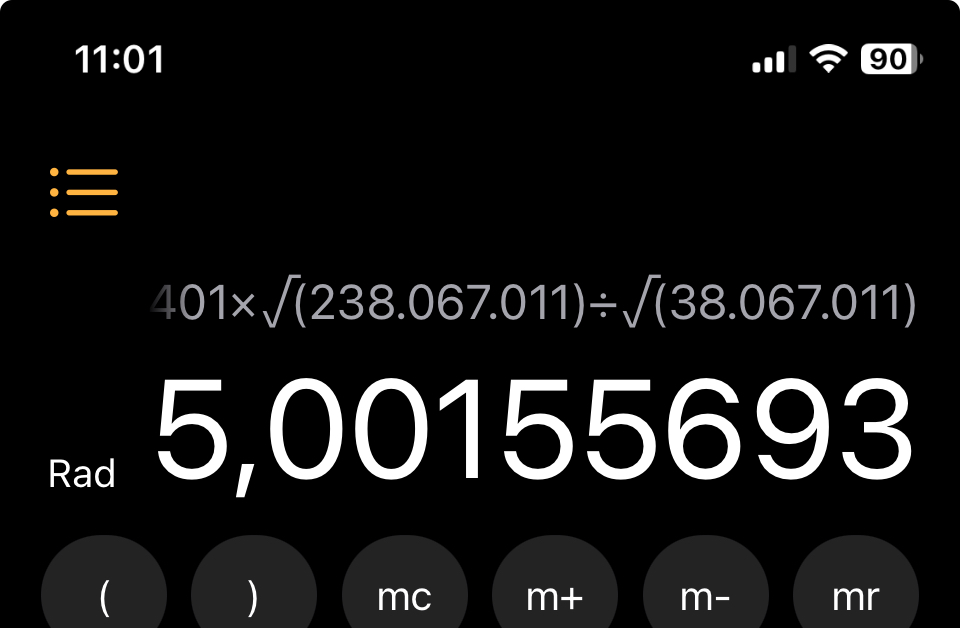
Also war das wohl ein Elektronenübergang von n = 5 auf n = 2, also die γ-Linie der Balmerserie des Wasserstoffspektrums:

Dazu braucht es dann wohl keine Schrödingersche Wellenfunktion ;-))
Vita Niels Bohr
- Herkunft und Jugend: Geboren am 7. Oktober 1885 in Kopenhagen. Er stammte aus einem intellektuellen Elternhaus; sein Vater war Physiologie-Professor. In seiner Jugend war er zudem ein begeisterter Fußballtorwart.
- Wissenschaftlicher Durchbruch (1913): Bohr entwickelte das nach ihm benannte Bohrsche Atommodell. Er kombinierte Rutherfords Kern-Modell mit der Quantentheorie von Max Planck und erklärte, dass Elektronen den Kern auf stabilen Bahnen umkreisen, ohne Energie zu verlieren.
- Nobelpreis (1922): Für seine Verdienste um die Erforschung der Struktur der Atome und der von ihnen ausgehenden Strahlung erhielt er den Nobelpreis für Physik.
- Institut für Theoretische Physik: Er gründete in Kopenhagen ein weltweit führendes Forschungszentrum, das Physiker wie Werner Heisenberg und Wolfgang Pauli anzog. Dort entstand die „Kopenhagener Deutung“ der Quantenmechanik.
- Zweiter Weltkrieg und Flucht: Da seine Mutter Jüdin war, musste Bohr 1943 vor der deutschen Besatzung aus Dänemark fliehen (über Schweden und London in die USA). Er war kurzzeitig am Manhattan-Projekt zum Bau der Atombombe beteiligt, wurde jedoch später zu einem engagierten Mahner für den Frieden.
- Spätes Wirken: Nach dem Krieg setzte er sich für die internationale Zusammenarbeit in der Atomforschung ein (z. B. Gründung des CERN) und erhielt 1957 den ersten „Atoms for Peace Award“.
- Tod: Niels Bohr starb am 18. November 1962 in Kopenhagen an den Folgen eines Schlaganfalls.
Wikipedia +13











